检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
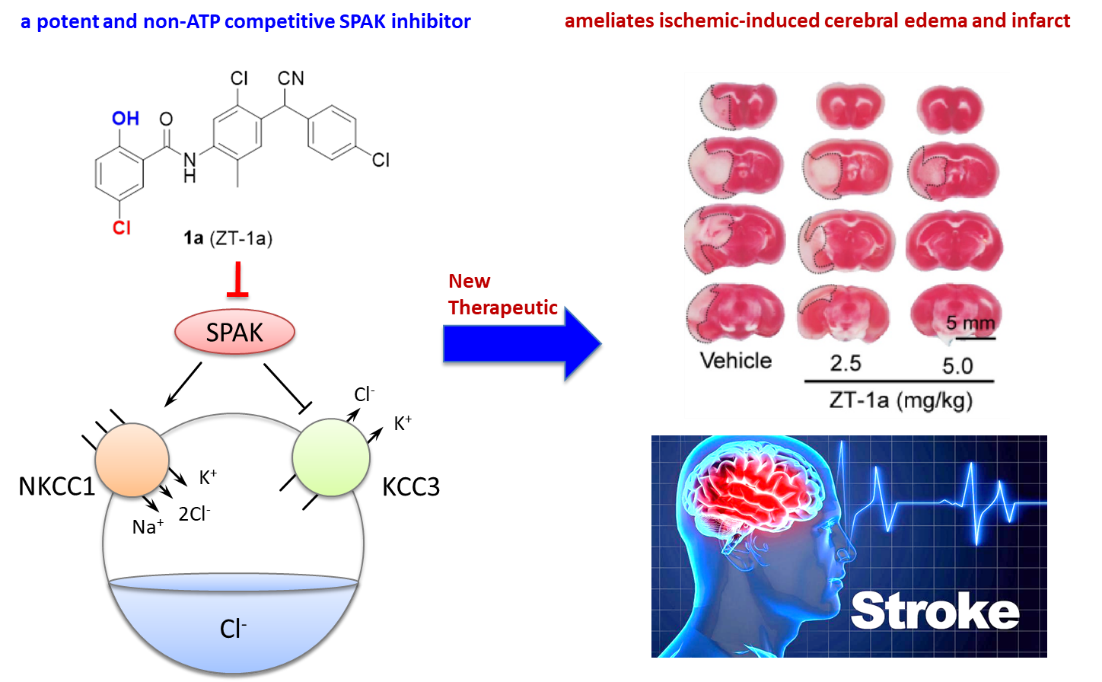
2020年1月7日,细胞应激生物学国家重点实验室、天然产物源靶向药物国家地方联合工程实验室、伟德BETVlCTOR1946邓贤明教授课题组在《Nature Communications》上合作发表题为“Modulation of brain cation-Cl− cotransport via the SPAK kinase inhibitor ZT-1a”的研究论文,首次报道了靶向未靶激酶SPAK的小分子抑制剂可有效改善缺血性中风后的神经功能,并能够改善脑出血后脑水肿和恢复脑水稳态。

缺血性中风通常是由大脑中的血块引起的,并可能在几分钟内导致脑死亡。中风后,细胞体积水平受损可导致大脑肿胀,这是颅骨切除术或脑脊液分流等高侵入性手术所引起的严重且难以治疗的并发症。另外,新生儿颅内出血是新生儿常见的严重疾病,脑室内出血常常导致出血后脑积水。目前,出血后脑积水的主要治疗方法为脑脊液分流术,但术后堵管和感染等并发症发生率较高。因此,临床上迫切需要寻找靶向药物干预策略,以期实现调节脑盐和水的稳态。针对上述难题,邓贤明教授教授课题组与英国埃克赛特大学医学院张金伟博士、耶鲁大学医学院神经外科医生Kristopher Kahle博士、匹兹堡大学医学中心神经内科学研究室孙丹丹教授组成联合研究团队对与脑盐和水稳态调节密切相关的阳离子-氯化物共转运蛋白(CCC)亚家族的蛋白质展开研究。在这项研究中,他们先是发现KCCs的抑制性磷酸化,如同NKCC1的磷酸化一样,在缺血性中风小鼠模型和出血后脑积水大鼠模型具有很显著的反馈作用,并受WNK-SPAK信号通路调控。接着开发了针对上述WNK-SPAK-CCC途径的化合物,ZT-1a,能有效和选择性地抑制SPAK激酶活性,发挥双重CCC调节功能(NKCC1抑制剂/ KCC活化剂)。在缺血性中风小鼠模型中,给予ZT-1a可以减轻缺血性中风引起的脑梗塞和水肿并改善神经功能。同时,在出血后脑积水大鼠模型中,给予ZT-1a可通过减少SPAK介导的脉络丛中NKCC1和KCC4的磷酸化来使出血性头颅的CSF分泌正常化。
因此,该化合物作为一种有效的激酶-共转运蛋白调节剂,可望用于治疗因颅脑外伤、缺血性中风、一氧化碳中毒或心脏骤停等损伤而导致的缺氧性脑损伤,或应用于恢复脑水稳态并改善神经功能,为发展针对中风患者或出血后脑积水患者的靶向治疗药物奠定基础。这一工作开启了未靶激酶在离子稳态相关的神经系统疾病治疗领域应用的探索。
邓贤明教授研究团队长期从事靶向蛋白激酶的小分子药物研究,尤其注重发展针对“未靶激酶(Untargeted Kinase)”的小分子抑制剂,并将其用于靶标的验证工作。张金伟博士团队主要关注WNK-SPAK-CCC信号通路的分子机制和生理病理学相关性。他们相识于各自在哈佛医学院Dana-Faber癌症研究所和英国MRC蛋白质磷酸化与泛素化研究所做博士后期间,长期以来密切合作,邓贤明教授团队主要负责激酶抑制剂的设计和优化,张金伟博士团队主要负责WNK-SPAK-CCC信号通路的分子机制研究和药效评价,形成了优势互补的学科交叉团队,并得到耶鲁大学医学院Kristopher Kahle博士和匹兹堡大学医学中心神经内科学孙丹丹教授在疾病模型方面的大力支持。
据悉,该论文由英国埃克赛特大学医学院、耶鲁大学医学院、匹兹堡大学医学中心、伟德国际官网登录入口生科院等单位合作完成,共同第一作者博士生张婷负责了该系列化合物的设计、合成与优化,张金伟博士、Kristopher Kahle博士、孙丹丹教授和邓贤明教授为共同通讯作者。该研究得到了科技部重点研发计划、国家自然科学基金委和中央高校基本科研业务费等的资助。
【邓贤明教授团队简介】
邓贤明教授团队针对重大疾病,以“首创药物(First-in-class therapeutics)”发现为目标,专注“未靶激酶”的药物发现化学生物学研究。近五年以通讯作者(或共同通讯)在Cell、Sci. Transl. Med.、J. Exp. Med.、Nat. Commun.、Cancer Res.、J. Med. Chem.等其它杂志发表SCI论文26篇。同时相关成果专利5项实现技术转让。
原文链接:https://www.nature.com/articles/s41467-019-13851-6
(伟德BETVlCTOR1946)