检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
在脊椎动物进化史上,髓鞘的出现让神经信号的传递变快了许多,人如果像无脊椎动物乌贼一样进化,人类的脊椎直径恐怕要粗过巨红杉树了。具有绝缘作用的髓鞘包裹神经轴突,从而使神经元间的动作电位进行快速地传导,此外,髓鞘还可以为神经元轴突提供代谢支持、物理保护和营养因子等,从而防止轴突退化。在中枢神经系统中,髓鞘是由少突胶质细胞生成的,而少突胶质细胞是少突胶质前体细胞(oligodendrocyte progenitor cell,OPC)分化而来。在一些脱髓鞘疾病中,如多发性硬化症和脑白质病变,在病发灶存在许多OPC,但它们不能分化成为成熟的少突胶质细胞,且我们对OPC分化形成髓鞘的认识依然不够深入,因此,深入探究OPC分化的因素对治疗这些疾病是非常重要的。
少突胶质细胞在分化时表面积变大了上千倍,需要经历非常活跃的货物运输。COPII介导了膜蛋白和可溶性蛋白从内质网到高尔基体的运输,COPII的功能异常会抑制蛋白分泌并对细胞分化和稳态产生影响,许多研究表明COPII成分与人类疾病之间存在联系,如Sec31突变导致严重的神经系统综合征。然而,目前COPII成分在少突胶质细胞分化和髓鞘形成中的生理功能和潜在机制尚不清楚。

2022年4月2号,我院张亮团队与附属第一医院王占祥团队合作在Journal of Clinical Investigation上发表题为Sec13 promotes oligodendrocyte differentiation and myelin repair through autocrine pleiotrophin signaling的研究成果,首次发现了COPII介导的自分泌在少突细胞分化和髓鞘再生中发挥重要的功能,为脱髓鞘相关疾病的治疗提供了新的思路。
该研究中,作者首先利用膜泡运输药物证实了COPII介导的膜泡运输有利于髓鞘生成,抑制COPII膜泡运输导致髓鞘再生能力降低。接着,作者构建了COPII蛋白Sec13的条件性敲除小鼠,在小鼠体内、离体环境和髓鞘损伤修复过程中均证实,Sec13是OPC分化形成髓鞘所必需的。
机制上,作者证明Sec13可通过PTN的自分泌而参与髓鞘生成的过程。作者发现分化的少突胶质细胞的条件性培养基可以促进OPC分化,利用液相质谱分析,检测到OPC分化过程中分泌蛋白增多,Sec13的缺失则导致这些蛋白分泌减少。在受Sec13调控的分泌蛋白中,其中PTN被分泌出来后可以显著促进OPC的分化,而突变了信号肽的PTN无法分泌出来发挥促进作用,PTN的分泌依赖于Sec13。此外,PTN可以回补Sec13敲低带来的OPC分化异常的表型,说明了Sec13调控髓鞘生成主要是通过PTN的分泌来实现。通过免疫共沉淀和蛋白免疫印迹实验,发现PTN作用于细胞膜受体PTPRZ1,引起P190的磷酸化,从而促进髓鞘生成。
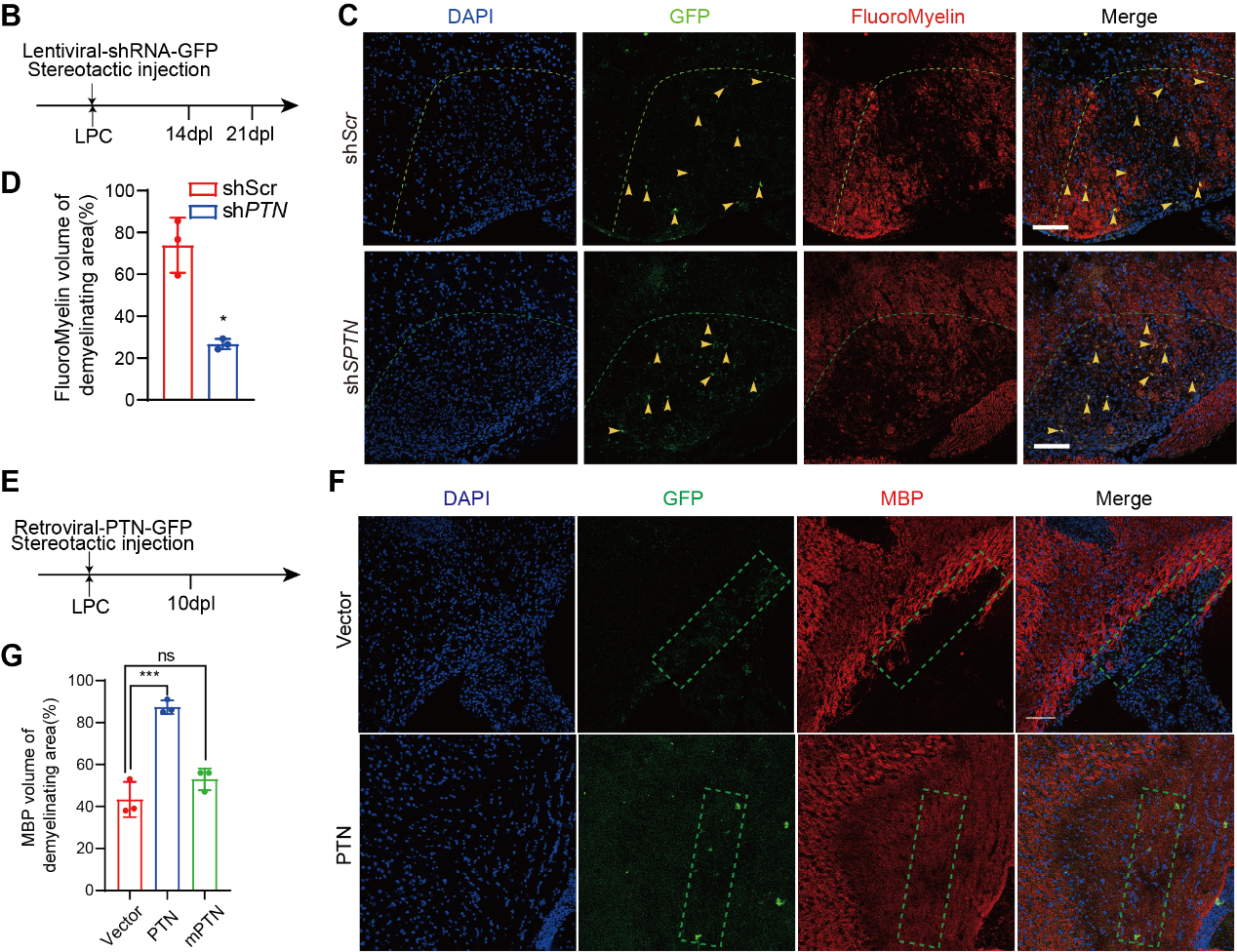
图1. PTN对髓鞘再生的影响
最后,在溶血卵磷脂诱导的髓鞘损伤模型中,作者发现髓鞘损伤后,PTN表达上调。利用病毒敲低PTN的表达,抑制髓鞘再生进程;相反,过表达PTN,可以促进髓鞘再生的速率。该研究通过原代细胞和小鼠模型阐述了COPII介导的膜泡运输在髓鞘生成过程中的生理功能,指出了PTN-PTPRZ1通路可能作为脱髓鞘疾病的治疗靶点。
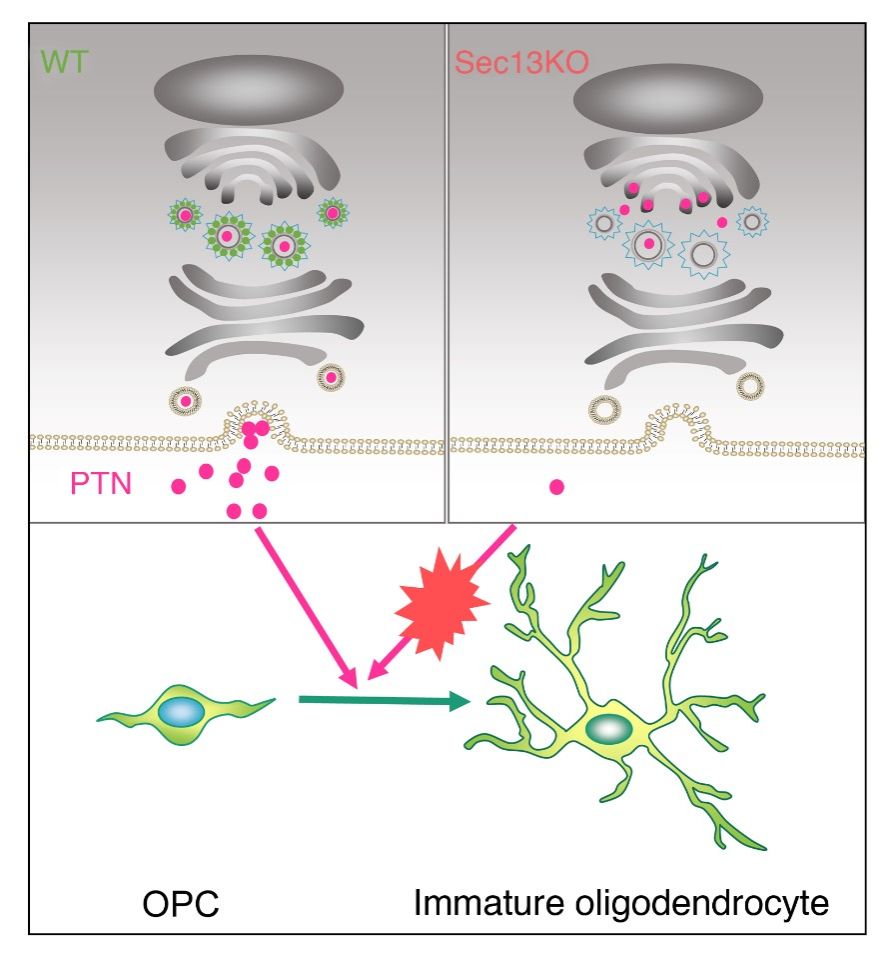
图2. COPII介导的自分泌因子PTN可以促进OPC分化形成髓鞘
该研究通讯作者为伟德BETVlCTOR1946张亮副教授和附属第一医院王占祥教授,伟德国际官网登录入口博士后刘志雄、博士生严旻标和硕士生雷婉莹为本文的共同第一作者。
原文链接:https://www.jci.org/articles/view/155096
(图/文张亮课题组)