检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
近日,陈航姿副教授和吴乔教授研究团队在《Molecular Cell》杂志上在线发表了题为“Nuclear Receptor Nur77 Facilitates Melanoma Cell Survival under Metabolic Stress by Protecting Fatty Acid Oxidation”的研究论文。该研究工作不仅揭示了核受体Nur77通过保护脂肪酸氧化关键酶TPβ免于氧化失活、保证葡萄糖饥饿状况下的脂肪酸氧化,从而促进细胞的存活的机制,也初步阐明脂肪酸氧化在黑色素瘤转移中的重要作用。
葡萄糖是肿瘤细胞最重要的能量来源,有氧糖酵解被认为是肿瘤代谢重编程的重要方式。为了适应体内恶劣的生长环境,肿瘤细胞还必须适时地切换能量来源以面对葡萄糖饥饿等代谢应激状态。脂肪酸是肿瘤的另一重要能量来源,然而关于葡萄糖饥饿等代谢应激状况下,肿瘤细胞调控脂肪酸氧化促进细胞存活的机制还很不清楚。
这项研究中,该团队首先发现Nur77对于黑色素瘤细胞适应葡萄糖饥饿的代谢应激状态至关重要。在葡萄糖饥饿下,Nur77可维持细胞内的NADPH及GSH的水平,从而降低葡萄糖饥饿引起的ROS,促进黑色素瘤细胞的存活。机制分析表明,葡萄糖饥饿可诱导ERK2的激活并磷酸化Nur77。磷酸化的Nur77被转运到线粒体,与执行脂肪酸氧化最后一步反应的硫解酶TPβ相互作用。TPβ在葡萄糖饥饿下会发生氧化修饰,从而抑制其酶活性,降低脂肪酸氧化。而当Nur77与TPβ结合后,由于Nur77自身对ROS介导的氧化修饰更敏感,Nur77以自我牺牲的方式保护TPβ免于氧化引起的失活。因而,Nur77与TPβ的结合促进脂肪酸氧化,从而维持NADPH、 GSH的水平,降低ROS,保证了细胞的存活。
为了进一步模拟肿瘤病理状况下的代谢应激,该团队采用了悬浮肿瘤细胞的模型。在悬浮状况(即细胞外基质粘附丧失)下,肿瘤细胞摄取葡萄糖的能力显著下降,而处于代谢应激的状态。Nur77及TPβ对黑色素瘤细胞在悬浮下的存活至关重要。进一步的小鼠实验表明,Nur77和TPβ通过提高循环肿瘤细胞(CTCs)在体内的存活,促进黑色素的转移。临床病例分析也表明,Nur77在复发的黑色素瘤中的表达水平明显高于原发的黑色素瘤。
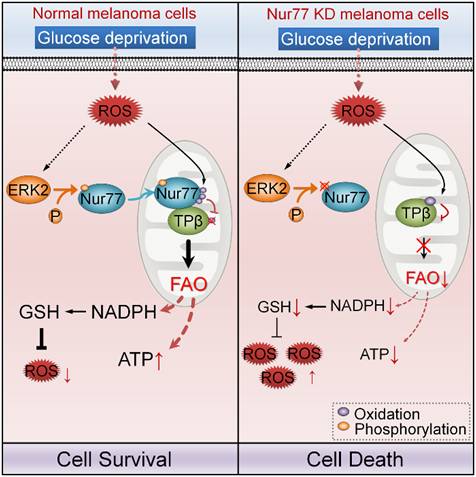
论文模式图
该研究不仅解释了黑色素瘤细胞适应代谢应激的机制,也说明了Nur77及脂肪酸氧化在黑色素瘤转移中的重要作用,为黑色素瘤的治疗提供了新思路。该论文的共同第一作者为硕士生李晓雪、王志静、郑宇以及博士生关运峰,通讯作者为陈航姿副教授和吴乔教授。该研究工作得到了国家自然科学基金、国家重点基础研发计划以及伟德国际官网登录入口校长基金的支持。
论文链接:http://www.cell.com/molecular-cell/fulltext/S1097-2765(18)30001-7
(伟德BETVlCTOR1946)